
암정보교육관
인체의 다양한 암
교모세포종이란?
교모세포종은 성인에서 발생하는 원발성 악성 뇌종양 중 가장 흔한 종양으로 진단 후 치료를 하지 않으면 3-6개월 내에 사망하고 각종 치료방법을 모두 동원하더라도 평균 생존기간이 12-14개월인 악성도가 매우 높은 질환이다.
우리나라에서는 매년 약 12,000명 정도의 뇌종양이 발생하는데 9,000여 명은 뇌수막종, 뇌하수체 선종과 같은 양성 종양이고 2,000여 명이 악성인데 교모세포종은 그 중 약 630명 정도가 매년 진단 되고 있다.
뇌조직의 신경교세포에서 기원하는 교모세포종은 주위 뇌조직으로 침습적 성장을 하므로 종양의 경계가 불분명하고 방사선학적 검사나 수술 시 실제 육안으로 관찰되는 경계보다 멀리까지 퍼져 있다. 뇌의 기능상 수술적 제거가 불가능한 부위에 위치한 경우가 많으며, 방사선치료로 완전 관해가 되지 않고, 뇌-혈관 장벽 때문에 항암제의 뇌 침투가 용이하지 않으므로 효과적인 항암제가 드물어 치료가 매우 어려워 나쁜 예후를 보이는 난치병이다.
The Cancer Genome Atlas 프로젝트의 첫번째 대상이 되었던 암종으로 포괄적 유전체적 특징이 잘 규명되어 있어 2016년부터 WHO 분류기준상 유전체 특징을 이용한 진단이 공식적으로 도입되었다.
증상
신경학적 증상은 두개강 내압 상승에 따른 일반적 증상과 종양의 뇌조직 침습 부위와 정도에 따른 국소증상으로 나타난다
가장 흔한 증상은 두통으로 지속적이며 시간에 따라 악화되고 특히, 국소적인 신경학적 증상이나 간질등과 동반된 경우에는 반드시 방사선학적 검사를 받아봐야 한다.
두개강 내압 상승에 따른 일반적 증상으로는 두통, 구토, 어지럼증, 인격과 지적 기능의 장애 및 간질 등의 증상이 나타난다. 급격한 뇌압 상승 증상을 보이는 경우의 원인으로는 종양 내 출혈, 부종, 뇌척수액의 순환장애 등이 있는데 이런 경우 응급조치가 필요하다.
종양에 의한 간질은 양상이 다양하며 간질 발작에서 회복하면 신경학적 이상 소견이 없는 경우가 흔하다. 교모세포종의 약 20%정도에서 초기 증상으로 간질이 나타난다.
종양의 뇌조직의 침습에 의한 국소증상으로는 운동마비, 보행장애, 언어장애, 뇌신경마비, 의식장애 등의 증상이 나타날 수 있다.
진단
뇌 자기공명영상 (MRI): 수술이나 조직학적 진단 전 기본이 되는 검사로 보다 정확한 진단과 평가를 위해서 기본적인 조영증강영상 외에도 확산강조영상, 조직관류영상 등 다양한 기법의 자기공명영상이 시도되고 있다.
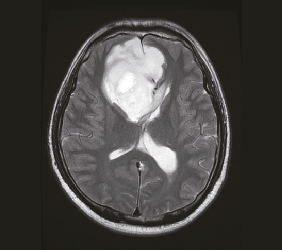
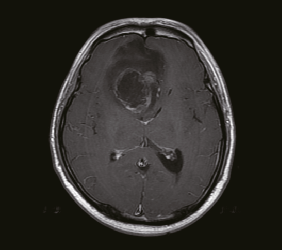
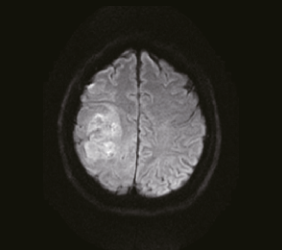
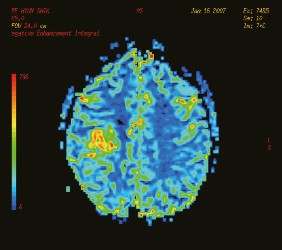
교모세포종의 자기공명영상 소견. 좌로부터 T2강조영상, T1조영증강영상, 확산강조영상, 조직관류영상
조직학적진단과 유전체진단: 조직학적진단이 가장 기본이 되는 확진 수단이며 IDH1/2와 TERT promoter 등의 변이 여부, EGFR 증폭여부, MGMT promoter의 메틸화 여부 등 종양조직의 유전체적 특징이 진단 및 예후 예측에 도움을 준다. 최근에는 관심유전자 조합으로 구성한 유전자패널이 진단에 이용되고 있다.
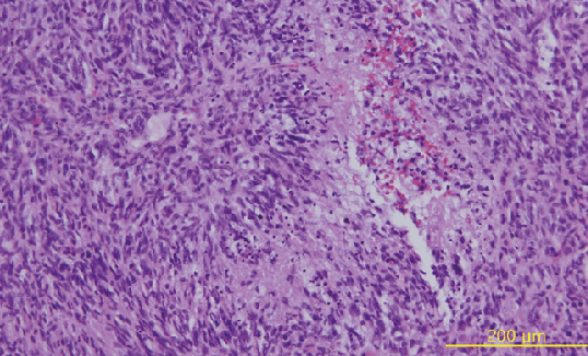
교모세포종의 대표적인 조직학적 소견. 비정형적인 악성도 높은 종양세포와 더불어 괴사, 혈관신생 등의 소견이 특징정임.

유전자패널 검사를 시행하는 차세대염기서열 분석기
De novo로 발생하는 1차 교모세포종과 저등급 교종으로부터 악성화 단계를 거쳐 발생하는 2차 교모세포종의 유전체적 특성 비교
| Primary glioblastoma | Seoondary glioblastoma | |||
|---|---|---|---|---|
| Clinical criteria® | Genetic criteria(IDH1) | Clinical criteria® | Genetic criteria(IDH1) | |
| Fraction in a population | 94.7% | 91.2% | 5.3% | 8.8% |
| Mean age, y | 59-62 | 56-61 | 33-45 | 32-48 |
| Male/female ratio | 1.33-1.5 | 1.2-1.46 | 0.65-2.3 | 1.0-1.12 |
| Mean clinical history, mo | 6.3 | 3.9 | 16.8 | 15.2 |
| Median overall survival, mo | ||||
| Surgery + radiotherapy | 4.7 | 9.9 | 7.8 | 24 |
| Surgery + radio/chemotherapy | 15 | 31 | ||
| Histologic features | ||||
| Oligodendroglial comp. | 18% | 20% | 42% | 54% |
| Necrosis | 89% | 90% | 63% | 50% |
| Genetic altrrations | ||||
| IDH1 mutations | 4-7% | 0% | 73-88% | 100% |
| TP53 mutations | 17-35% | 19-27% | 60-88% | 76-81% |
| ATRX mutations | 4-7% | 57-80% | ||
| EGFR amplification | 36-45% | 35-39% | 0-8% | 0-6.5% |
| CDKN2A deletion | 31-52% | 30-45% | 19-20% | 7-22% |
| PTEN mutations | 23-25% | 24-26% | 4-12% | 0-8% |
| 19q loss | 6% | 4% | 45% | 32% |
| 1q/19q loss | 2-8% | 0-13% | ||
| 10p loss | 47% | 67% | 8% | |
| 10q loss | 70% | 63% | 73% | |
치료
현재 교모세포종에서 널리 인정되고 있는 표준치료법은 다음과 같다.
| 종양 종류 | 최초 진단시 | 재발시 |
|---|---|---|
| 교모세포종, WHO Gr Ⅳ(나이<65-70) | 절제 또는 생검 + 테모졸로마이드 동시화학방사선조가 + 테모졸로마이드 보조화학요법 | 재수술 + 방사선재조사, 테모졸로마이드 재투여 또는 베바시주맵 |
| 교모세포종, WHO Gr Ⅳ(나이>65-70) | 절제 또는 생검 + 방사선 치료 또는 테모졸로마이드 보조화학요법 또는 병용 치료(MGMT와 KPS에 따라) | 재수술 + 화학요법 또는 방사선재조사 |
| 화학요법 종류 | 용량과 투여방법 | |
| 테모졸로마이드(temozolomide) | 150-200mg/m²,걍구,5days/wk x 4wk | |
| 베바시주맵(bevacizumab) | 10mg/kg f 또는 2wk 또는 15mg/kg f또는 3wk | |
수술적 치료
교모세포종에서 수술적 치료의 목적은 정확한 조직학적 진단을 통해 종양의 성격을 분석, 파악하여 향후 치료 계획에 이용하고, 뇌압상승과 뇌조직 압박에 의한 신경학적 증상을 개선하며, 종양 새포를 가능한 한 줄여줌으로써 방사선치료 및 항암요법의 치료효과를 증대 시키는 것이다, 현대에서는 종양을 최대한 그리고 안전하게 절제하기 위해 형광유도수술, 뇌항해기법장치, 수술 중 전기생리학적 모니터링, 각성수술 등 다양한 수술 보조 기술들이 적용 되고 있다.
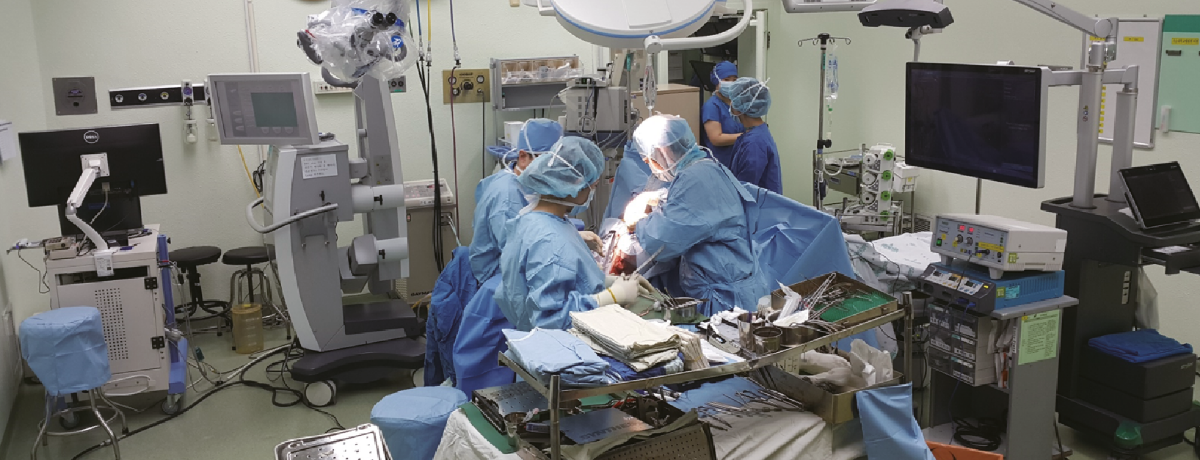
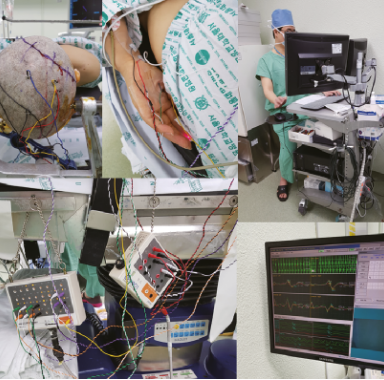
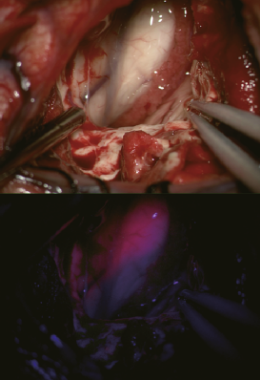
뇌종양 수술 광경. 하단 좌로부터 수술 중 전기생리학적모니터링 , 형광유도수술, 뇌항해기법.
방사선 치료
수술 후 남아있는 종양을 소멸하고 종양의 성장을 지연시켜 환자의 증상을 완화, 기능장애의 회복, 국소적 치유, 재발 방지를 목적으로 수술적 치료 이후에 시행한다. 대개 총 방사선 량 60Gy정도를 6주 동안 분할하여 조사하는 스케쥴로 시행하는 것이 보통이나 다양한 임상적 조건에 따라 조사량과 기간에 변화를 주는 변형된 방사선 치료가 시도되고 있기도 하다.
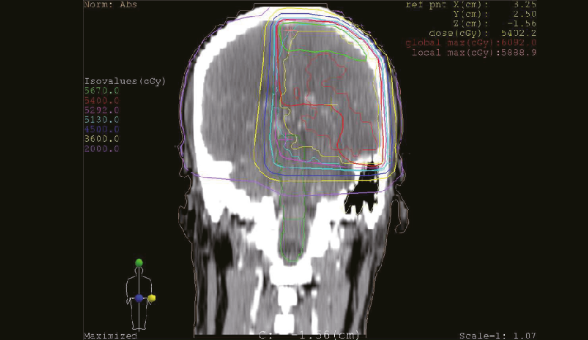
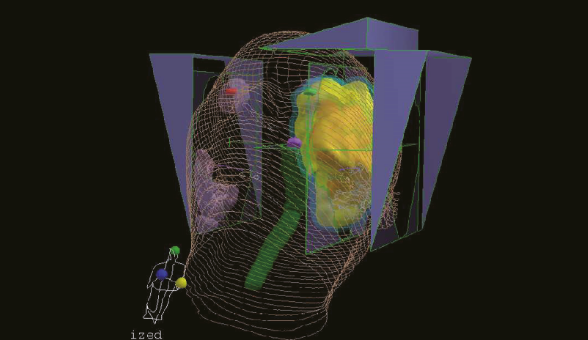
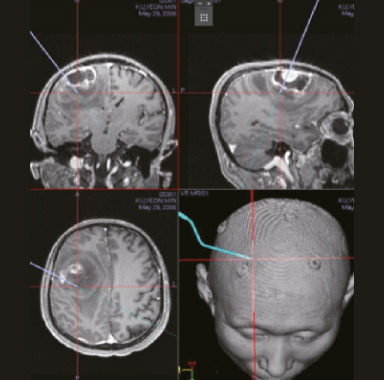
교모세포종에서 방사선 치료 선량계획 모식도.
항암화학요법
교모세포종에의 치료에 있어서 수술 및 방사선 치료는 그 효과가 입증이 되어 있으나 완치에 이르게 하지는 못하기 때문에 역사적으로 다양한 항암화학요법을 시도해 왔으나 제한적인 효과만을 보아 왔다. 현재 테모졸로마이드를 이용한 방사선-항암치료 병용요법은 교모세포종의 표준치료이며 그 외 다양한 항암제들이 개발되어 임상시험을 통해 검증을 받고 있으나 아직은 표준치료를 대체할 만한 약제는 없는 실정이다.
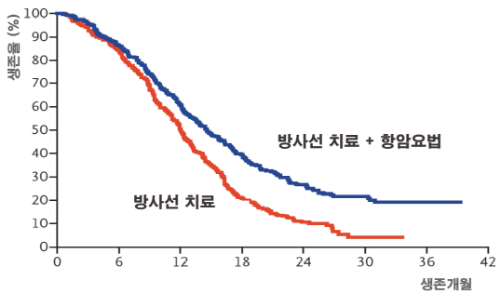
교모세포종에서 수술 후 방사선치료와 항암치료를 병용한 표준치료법과 방사선치료만 했을 경우의 생존률 차이.
